Saúde em alerta:
reuso de produtos e infecções
Aurimar José Pinto*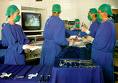 A Agência Nacional de Vigilância Sanitária (Anvisa) pretende limitar o número de procedimentos cirúrgicos diários, especialmente os que usam pequenas câmeras de vídeo introduzidas no paciente, para reduzir o número de infecções. A nova medida que a Anvisa parece querer adotar em breve em hospitais e clínicas tem o objetivo de reduzir o número de infecções pós-cirúrgicas provocadas pela
A Agência Nacional de Vigilância Sanitária (Anvisa) pretende limitar o número de procedimentos cirúrgicos diários, especialmente os que usam pequenas câmeras de vídeo introduzidas no paciente, para reduzir o número de infecções. A nova medida que a Anvisa parece querer adotar em breve em hospitais e clínicas tem o objetivo de reduzir o número de infecções pós-cirúrgicas provocadas pela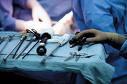 Micobactéria de Crescimento Rápido (MCR), proveniente de problemas na limpeza e esterilização de instrumentos e aparelhos utilizados
Micobactéria de Crescimento Rápido (MCR), proveniente de problemas na limpeza e esterilização de instrumentos e aparelhos utilizados
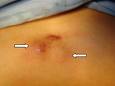
De acordo com matérias publicadas em veículos de comunicação, o surto pela "micobacteria massiliensis", que já atingiu os Estados do Espírito Santo, Rio de Janeiro e Minas Gerais, é causado por falha na limpeza de instrumentos cirúrgicos e pode atingir qualquer tipo de procedimento cirúrgico.
Embora não haja clareza quanto ao surto estar ou não relacionado apenas com os instrumentos de uso permanente, esse movimento acende, mais uma vez, luz vermelha para uma questão muito séria no setor de saúde brasileiro: a reutilização de produtos médico-hospitalares.
Diante desse quadro, a Associação Brasileira dos Importadores de Equipamentos, Produtos e Suprimentos Médico-Hospitalares (Abimed) faz mais uma vez um alerta público sobre os riscos para a saúde decorrentes da utilização de dispositivos médico-hospitalares fabricados para uso único reprocessados e reutilizados que podem gerar infecções, já que seus projetos não levaram em consideração a possibilidade de reprocessamento para permitir múltiplo uso.
O reprocessamento de produtos cirúrgicos, mesmo os de uso único, é uma prática realizada nas instituições de saúde brasileiras. A reutilização de materiais nos hospitais e centros médicos é um assunto complexo e com grande potencial danoso para a saúde tanto dos pacientes quanto dos profissionais que os manuseiam nas intervenções cirúrgicas nos processos de limpeza, desinfecção e esterilização.
A Anvisa revisou a legislação sobre o reprocessamento com a edição de três novas resoluções: a RDC 156/06 e as REs 2605/06 e 2606/06. A RE 2605/06 lista cerca de 100 produtos médicos de uso único cujo reprocessamento não é permitido. Já a RE 2606/06, que estabelece parâmetros como guia de protocolos a serem adotados pelos estabelecimentos que fazem o reprocessamento, visando garantir a segurança e a eficácia dos produtos reprocessados, estabeleceu a data limite de agosto de 2007 para implantar os protocolos. Esta data foi postergada para fevereiro de 2008, através da RE 2305, de julho de 2007. Somente em dezembro de 2007, através da Portaria 1001 da Anvisa, foi criado um Grupo de Trabalho para regulamentar as atividades dos serviços que realizam reprocessamento cujo prazo também se extinguiu em 03 de junho de
O problema está nos produtos não inclusos nessa lista de produtos de uso único. De acordo com a resolução, os materiais que não estiverem na lista poderão ser reutilizados ou reprocessados, obedecendo a Protocolos a serem desenvolvidos pelas empresas de serviços e aprovados pela Anvisa, cujos critérios não nos parecem bem estabelecidos. Trata-se de uma questão polêmica, pois os fabricantes são claros de que não têm como garantir a segurança dos seus produtos após o primeiro uso, e esta responsabilidade, conforme a atual regulamentação é total das entidades de serviços que os reprocessam.
Na opinião dos fabricantes importadores, os produtos de uso único não devem ser reprocessados. Não existe viabilidade técnica para uma fiscalização eficiente nem garantia de segurança da vida do paciente em casos de reuso. O reprocessamento de produtos de uso único é admitido porque, conforme consideração na RDC 156, “a reutilização de produtos médicos rotulados para uso único tem sido uma prática largamente encontrada nos serviços de saúde do Brasil e do exterior”.
O principal problema a nosso ver é o fato da Anvisa legalizar uma atividade que representa risco para a saúde da população ao mesmo tempo que sabemos que é difícil sua fiscalização. O reuso de materiais que foram desenvolvidos para serem usados uma única vez contribuem com a infecção cruzada e à adquirida em hospitais.
Na atual regulamentação não há nenhuma menção à necessidade de o paciente ser comunicado previamente, da possibilidade de uso de um produto médico reutilizado. Temos denunciado uma clara ignorância da legislação aos princípios éticos relacionados com os direitos dos pacientes e as conseqüências legais em cadeia no caso de danos ao paciente tratado com dispositivos médicos de uso único reprocessados. A falta de clareza de como a Anvisa poderá efetivamente fiscalizar o reprocessamento desses produtos, preocupa toda a cadeia do setor de saúde.
Estudos de várias fontes demonstram que o reprocessamento de produtos destinados a uso único pode afetar a funcionalidade dos mesmos, com sérios riscos aos pacientes, tais como:
- resíduos da utilização anterior como sangue e seus componentes, secreções e outros componentes corpóreos, que podem resultar em 'sujeira' estéril, podendo levar, entre outras implicações mais graves, a reações alérgicas, e/ou resíduos de agentes de limpeza ;
- alterações nas propriedades físicas, químicas ou funcionais dos dispositivos médicos reprocessados, que podem falhar durante um procedimento cirúrgico, ou mesmo romper-se dentro do corpo do paciente;
- dificuldade de rastreabilidade dos produtos reutilizados, contrariando a própria definição do que vem a ser uma "vigilância" sanitária.
Apesar da atual regulamentação prever que as entidades prestadoras de serviços hospitalares sejam responsáveis e elaborem e validem seus protocolos, a Abimed entende que os atuais fatos de contaminação vêm atestar o que já se comenta há muito tempo. O reuso é um perigo iminente de infecção hospitalar. Temos receio de que as ações da Anvisa em querer limitar e restringir o número de procedimentos e equipamentos, não seja suficiente e vá na contramão da sua própria missão, que é proteger e promover a saúde da população, garantindo a segurança sanitária de produtos. Além disso, coloca a vida de todos os brasileiros numa verdadeira roleta-russa.
Todo o setor de saúde deve estar muito atento para evitar que mais pacientes sejam vítimas, por conta do reuso de produtos médicos. Empresas fabricantes e distribuidoras devem reforçar junto aos seus clientes e prestadores de serviços a responsabilidade que têm para com a qualidade dos produtos reprocessados. Hospitais, clínicas e todos os profissionais envolvidos no setor de saúde devem averiguar a procedência dos produtos. Utilizar produtos reprocessados já é por si só um risco aos pacientes, muito mais sem a certeza de cumprimento dos procedimentos estabelecidos pelas regulamentações da Anvisa. Cada cidadão, profissional ou paciente, deve considerar-se usuário potencial, e como tal, servir de agente fiscalizador dessa prática. Segundo registros do Sistema Único de Saúde (SUS), cerca de 30% dos pacientes internados em todo o País contraem algum tipo de infecção hospitalar. Só em 2007, o Rio de Janeiro registrou 416 casos de infecções causadas pela micobactéria de crescimento rápido (MCR). Em oito anos, foram 969 vítimas. O Rio também lidera o ranking de hospitais contaminados, sendo que das 128 unidades infectadas, 77 ficavam no Estado carioca. O Espírito Santo registrou a contaminação em 14 hospitais. Segundo informações do Jornal do Brasil, a Associação de Estudos em Controle de Infecção Hospitalar do Estado do Rio (AECIHERJ) informou que 80% das infecções por MCR ocorreram em hospitais particulares, porque costumam ter mais equipamentos de videocirurgias - mais suscetíveis à contaminação por esse tipo de bactéria. O SUS registra que 30% dos pacientes contraem infecção hospitalar
Crédito:Cris
Autor:Caio Prates
Fonte:Universo da Mulher